Wetenschappers hebben een baanbrekend kunstmatig intelligentiemodel ontwikkeld dat artsen helpt bij de diagnose van zeldzame genetische aandoeningen. Het model, genaamd popEVE, maakt gebruik van evolutionaire informatie uit tienduizenden soorten én grote menselijke genetische databanken om eerder onbekende mutaties te identificeren als potentieel ziekmakend.
Achtergrond en aanpak
Tot nu toe bleef het in veel gevallen lastig om de impact van zogenaamde “missensemutaties” te beoordelen — mutaties die slechts één aminozuur in een eiwit veranderen. Het nieuwe model koppelt deze variantie aan evolutionaire patronen die aantonen hoe eiwitten zich door miljoenen jaren hebben ontwikkeld, én aan gegevens over hoe gezonde mensen genetisch variëren.
New AI model enhances diagnosis of rare diseasesPopEVE system outperformed rivals such as Google DeepMind’s AlphaMissense |
Resultaten die indruk maken
In een test van 513 kinderen met ernstige ontwikkelingsstoornissen, waarbij de mutatie volledig nieuw was, wist popEVE in 98% van de gevallen de meest schadelijke mutatie correct aan te wijzen. Bovendien identificeerde het model 123 genen die voorheen niet aan ziekten werden gekoppeld, maar wel actief zijn in de hersenontwikkeling.
|
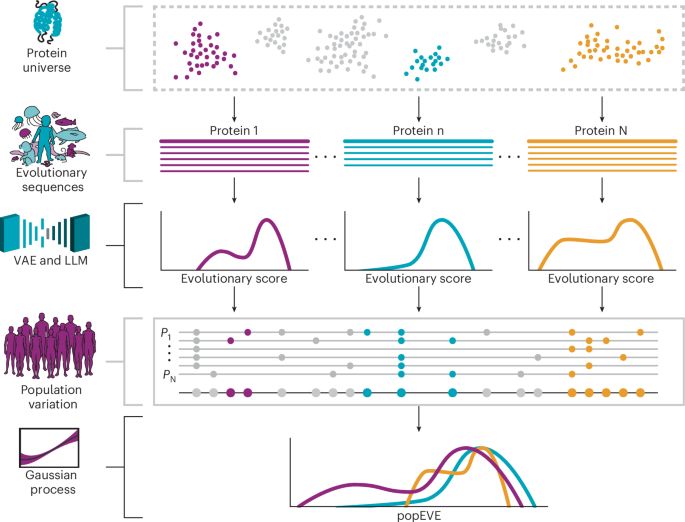
Proteome-wide model for human disease genetics - Nature GeneticsMissense variants remain a challenge in genetic interpretation owing to their subtle and context-dependent effects. Although current prediction models perform well in known disease genes, their scores are not calibrated across the proteome, limiting generalizability. To address this knowledge gap, we developed popEVE, a deep generative model combining evolutionary and human population data to estimate variant deleteriousness on a proteome-wide scale. popEVE achieves state-of-the-art performance without overestimating the burden of deleterious variants and identifies variants in 442 genes in a severe developmental disorder cohort, including 123 novel candidates. These genes are functionally similar to known disease genes, and their variants |
Waarom dit een gamechanger kan zijn
- Het model overtrof rivalen zoals DeepMind’s AlphaMissense op meerdere meetpunten — bijvoorbeeld in de toepassing bij niet-Europese populaties.
- Omdat het relatief weinig rekenkracht vereist, is het ook geschikt voor gezondheidszorg in lage- en middeninkomenslanden — iets waar genetische diagnostiek vaak stokt.
- Het stelt artsen nu in staat ook mutaties zonder bekend parent-DNA (ouders) te challengen – een stap vooruit in de klinische toepassing van genomica.

|
A new AI model called popEVE can predict how likely each variant in a patient’s genome is to cause disease.
|
Kritische kanttekeningen en de weg vooruit
Hoewel de resultaten indrukwekkend zijn, blijft popEVE voorlopig als hulpmiddel gelden — geen definitief klinisch oordeel. Er is nog validatie nodig in grotere, klinische settings, en uiteraard aandacht voor ethische, privacy- en toegankelijkheidsvraagstukken. Maar dit onderzoek toont aan dat AI niet enkel een hype is in genetica, maar steeds concreter een rol speelt in de praktijk van de zeldzame ziektes.
Slotwoord – Wat dit betekent
Voor patiënten met zeldzame genetische aandoeningen kan deze ontwikkeling betekenen dat er sneller, preciezer en wereldwijd diagnostiek mogelijk wordt. Voor technologie- en webdesign-professionals opent het nieuwe perspectieven over hoe AI-modellen worden gebouwd, gevalideerd én toegepast — met relevante lessen voor jouw content-strategie (denk: toegankelijkheid, diversiteit, schaalbaarheid).









