Een nieuw hoofdstuk in de biologie
Wetenschappers hebben een baanbrekend kunstmatig-intelligent model ontwikkeld dat ons DNA niet alleen leest, maar ook interpreteert — een doorbraak die de manier waarop we genetische informatie begrijpen kan veranderen. Het AI-systeem, AlphaGenome geheten, is ontworpen door onderzoekers van Google DeepMind en werd onlangs beschreven in Nature.
Terwijl het menselijk genoom uit meer dan drie miljard “letters” bestaat — en slechts ongeveer 2% daarvan de bekende eiwitten codeert — bleef die overige 98%, het zogenaamde donkere genoom, een mysterie, vol met varianten die een rol kunnen spelen in ziektes zoals kanker, diabetes en hoge bloeddruk. AlphaGenome analyseert nu stukken DNA van maar liefst 1 miljoen letters tegelijk, wat onderzoekers een ongekend gedetailleerd beeld geeft van genetische functionaliteit.
Hoe AI de code van het leven ontrafelt
In tegenstelling tot veel AI-systemen die voorspellende tekst genereren zoals ChatGPT, werkt AlphaGenome fundamenteel anders. Het is een sequence-to-function-model: het kijkt naar de betekenis van sequenties en voorspelt hoe veranderingen in de DNA-code de werking van genen en hun regulatie beïnvloeden.
Dat stelt biologen in staat om te voorspellen wat er gebeurt als één enkele “letter” in het DNA verandert — cruciaal voor het begrijpen van genetische ziekten en mogelijk ook voor het ontwerpen van therapeutische interventies. Door de effecten van varianten te simuleren, kunnen onderzoekers sneller bepalen welke mutaties leiden tot ziekteprocessen en welke nauwelijks effect hebben.
|
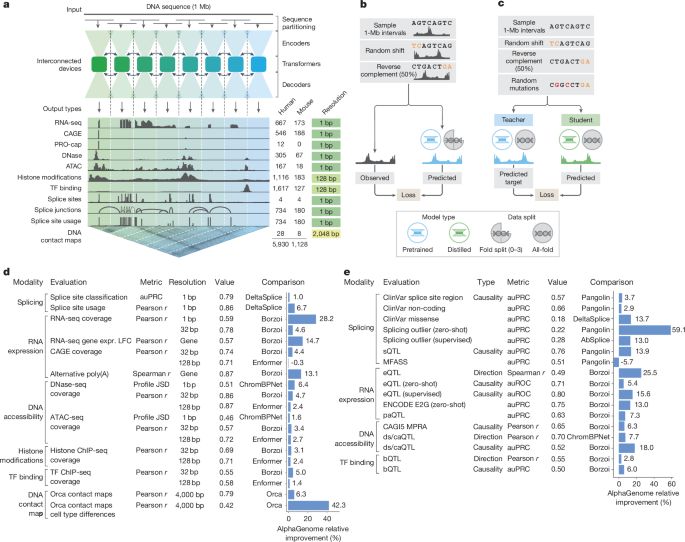
Advancing regulatory variant effect prediction with AlphaGenome - NatureDeep learning models that predict functional genomic measurements from DNA sequences are powerful tools for deciphering the genetic regulatory code. Existing methods involve a trade-off between input sequence length and prediction resolution, thereby limiting their modality scope and performance1–5. We present AlphaGenome, a unified DNA sequence model, which takes as input 1 Mb of DNA sequence and predicts thousands of functional genomic tracks up to single-base-pair resolution across diverse modalities. The modalities include gene expression, transcription initiation, chromatin accessibility, histone modifications, transcription factor binding, chromatin contact maps, splice site usage and splice junction coordinates and strength. Trained |
Van puzzelstukje naar medicijnontwikkeling
Experts noemen AlphaGenome een “grote sprong vooruit” voor de biologie. Waar klassieke methoden vaak lang en duur zijn, geeft deze AI-benadering een veel duidelijker beeld van de gene regulatory networks — de ingewikkelde systemen van genexpressie, chromatinestructuur en DNA-splicing die bepalen hoe onze cellen functioneren.
Dat betekent dat wetenschappers nu kunnen nagaan welke genetische varianten daadwerkelijk ziekten veroorzaken en welke slechts “bijproducten” zijn van evolutionaire geschiedenis. Deze inzichten zouden de zoektocht naar nieuwe medicijntargets kunnen versnellen, met toekomstmogelijkheden in gepersonaliseerde geneeskunde en synthetische biologie.
Kritische geluiden en grenzen van de AI
Hoewel de vooruitgang indrukwekkend is, waarschuwen onderzoekers dat AlphaGenome niet perfect is. Voorspellingen over hoe DNA-elementen over grote afstanden met elkaar interageren zijn nog minder betrouwbaar, en er is werk nodig om de accuraatheid voor verschillende celtypen te verbeteren. De genetische instructies die een hartcel anders maken dan een hersencel zijn subtiel en complex — en AI moet nog leren deze verschillen scherp te onderscheiden.
AI model from Google DeepMind reads recipe for life in our DNAIt could transform our understanding of why diseases develop and the medicines needed to treat them, says researchers. |
Een genetische revolutie in zicht
DeepMind’s AlphaGenome vertegenwoordigt een nieuw paradigma: AI die niet alleen menselijke taal en beelden begrijpt, maar ook de fundamentele instructies van het leven zelf. Door de zwarte doos van het donkere genoom te openen, staan we aan de vooravond van een periode waarin genetische ziekten eerder kunnen worden gedetecteerd, beter begrepen en mogelijk zelfs geneutraliseerd.









